Dopo molteplici studi per verificarne la sicurezza e l’efficacia, e dopo un acceso dibattito, la somministrazione è iniziata, ma solo per i pazienti “eleggibili” al trattamento.
Anticorpi monoclonali: quali sono quelli utilizzabili
Nel
parere della Commissione Tecnico Scientifica (CTS) di AIFA, adottato il
4 febbraio 2021, viene specificato che “la CTS, pur considerando l’immaturità dei dati e la conseguente incertezza rispetto all’entità del beneficio offerto da tali farmaci, ritiene, a maggioranza, che in via straordinaria e in considerazione della situazione di emergenza, possa essere opportuno offrire comunque un’opzione terapeutica ai
soggetti non ospedalizzati che, pur avendo una
malattia lieve/moderata risultano
ad alto rischio di sviluppare una forma grave di COVID-19 con conseguente aumento delle probabilità di ospedalizzazione e/o morte. Si tratta, in particolare, di un setting a rischio per il quale attualmente non è disponibile alcun trattamento standard di provata efficacia”. Questo parere, consultabile sul portale istituzionale, fu fornito per verificare le possibili modalità di utilizzo di tali farmaci all’interno del Servizio sanitario nazionale.
Il
10 marzo AIFA ha comunicato l’attivazione web e la pubblicazione delle
schede di monitoraggio del Registro Anticorpi monoclonali per COVID-19, specificando che:
- L'uso degli anticorpi monoclonali è autorizzato in soggetti di età >12 anni, positivi per SARS-CoV-2, non ospedalizzati per COVID-19, non in ossigenoterapia per COVID-19, con sintomi di grado lieve-moderato di recente insorgenza (e comunque da non oltre 10 giorni) e presenza di almeno un fattore di rischio (o almeno 2 se uno di essi è l’età >65 anni). Se il paziente è già inserito, o in procinto di esserlo, in una sperimentazioni clinica e/o in un programma di uso compassionevole (anche nominale) non deve essere inserito nel presente registro AIFA.
A partire dal
18 marzo 2021 è possibile dispensare anche la seguente combinazione
scheda di dispensazione dei farmaci monoclonali: 1 flaconcino di bamlanivimab da 700 mg/20 ml + 2 flaconcini di etesemivab da 700 mg/20 ml.
La
scheda di dispensazione dei farmaci monoclonali, riporta quali sono ora gli utilizzabili.

Anticorpi monoclonali: il percorso organizzativo della Toscana
Varie Regioni hanno iniziato ad autorizzare la somministrazione degli anticorpi monoclonali per la terapia contro Covid-19.
La Toscana nel
decreto del 19 marzo 2021 Approvazione del percorso organizzativo necessario a garantire la corretta individuazione e gestione dei pazienti candidabili al trattamento con gli anticorpi monoclonali fornisce dettagliate indicazioni, di cui riportiamo solo alcuni punti salienti.
Bamlanivimab,
etesevimab, prodotti dall’azienda farmaceutica Eli Lilly, e
casirivimab e
imdevimab, prodotti dall’azienda farmaceutica Regeneron/Roche, sono anticorpi monoclonali progettati per legarsi alla proteina spike di SARS-CoV-2 in modo da impedire al virus di penetrare nelle cellule dell'organismo. Legandosi a diverse parti della proteina spike, il loro utilizzo in associazione (bamlanivimab-etesevimab e casirivimab-imdevimab) può avere un effetto maggiore rispetto all'uso in monoterapia. Al momento risultano in corso di studio numerosi anticorpi monoclonali prodotti da diverse Ditte farmaceutiche e in fase di approvazione da parte degli enti regolatori internazionali e nazionali.
Questi i criteri di selezione dei pazienti che possono ricevere la terapia.

Questo è il grafico che mostra come avviene la presa in carico dei pazienti.
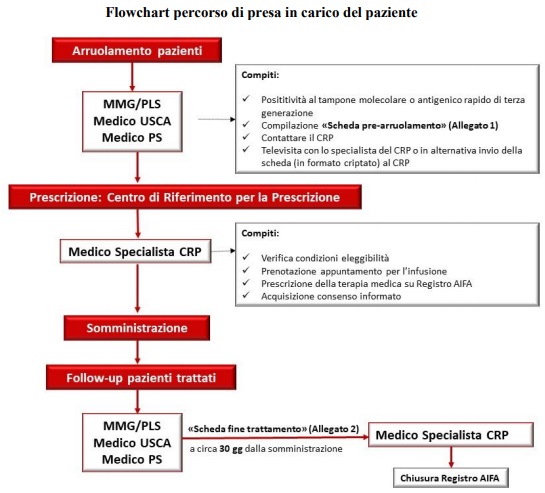
In elenco i centri abilitati alla prescrizione.

Sebbene i vaccini siano la speranza per una vittoria definitiva contro Covid-19 e per un ritorno alla “normalità”, le terapie sono in questo momento indispensabili. Grazie quindi anche a chi ha studiato e a chi ha reso possibile l’utilizzo degli anticorpi monoclonali.
immagine:
vectorjuice - it.freepik.com 




