La rivista “
Morbidity and Mortality Weekly Report” ha pubblicato alla fine della scorsa settimana
due studi preliminari sulla sicurezza e l'efficacia del vaccino Pfizer/BioNTech COVID-19 nei bambini e negli adolescenti.
Vaccini anti Covid-19 nei bambini: quanto sono sicuri?
Nel
primo studio, i ricercatori dei Centri statunitensi per il controllo e la prevenzione delle malattie (
CDC) hanno
analizzato i dati del
Vaccine Adverse Event Reporting System (VAERS) e dell'
app per smartphone v-safe dei genitori, sugli
eventi avversi nei bambini di età compresa tra 5 e 11 anni dal 3 novembre al 19 dicembre 2021. L'
età media era di 8 anni e il 44,6% erano maschi.
Gli eventi avversi gravi sono stati definiti come quelli che richiedono il ricovero in ospedale o lunghe degenze ospedaliere e quelli che mettono a rischio la vita o portano a invalidità permanente, o morte.
VAERS ha ricevuto
4.249 segnalazioni di eventi avversi dopo la somministrazione di 8,7 milioni di dosi di vaccino COVID-19 a bambini di età compresa tra 5 e 11 anni:
- 4.149 (97,6%) segnalazioni VAERS erano per eventi non gravi
- 100 (2,4%) erano per eventi gravi.
Gli
eventi non gravi segnalati più comunemente erano
correlati alla somministrazione del vaccino (alcuni senza alcun evento avverso), includendo nessun evento avverso (1.157; 27,9%), problemi di preparazione del prodotto (925; 22,3%) e dose somministrata errata (675; 16,3%)
L'
età media dei bambini con segnalazioni di eventi gravi era di
9 anni e 61 (61,0%) segnalazioni erano tra i maschi.
Le condizioni e i risultati diagnostici più frequentemente riportati
tra le 100 segnalazioni di eventi gravi erano:
- febbre (29; 29,0%)
- vomito (21; 21,0%)
- aumento della troponina (15; 15,0%)
- tra i 12 casi gravi di convulsioni:
- 1 bambino ha avuto sincope (perdita di coscienza dopo un calo della pressione sanguigna)
- 1 altro potrebbe aver avuto sincope
- 2 bambini hanno avuto una crisi convulsiva correlata alla febbre
- 1 bambino ha avuto una storia di convulsioni
- 2 potrebbero aver avuto un disturbo convulsivo in evoluzione
- 5 avevano convulsioni di nuova insorgenza
- tra 15 segnalazioni preliminari di miocardite identificate durante il periodo considerato:
- 11 sono state verificate e hanno soddisfatto la definizione del caso per miocardite; di questi 11 bambini, 7 si sono ripresi e 4 si stavano riprendendo al momento del rapporto.
VAERS ha ricevuto due segnalazioni di morte durante il periodo analitico;
entrambi sono in fase di revisione. Questi decessi si sono verificati in due femmine, di 5 e 6 anni, entrambe con storie mediche complicate ed erano in salute fragile prima della vaccinazione. Nessuno dei dati ha suggerito un'associazione causale tra morte e vaccinazione.
Dei
42.504 bambini di questa fascia di età arruolati in v-safe:
- il 57,5% ha avuto reazioni locali
- il 40,9% ha avuto reazioni sistemiche, inclusi dolore al sito di iniezione, affaticamento e cefalea.
Nella
settimana successiva al ricevimento della prima dose di vaccino:
- il 54,8% dei bambini ha avuto reazioni locali
- mentre il 34,7% ha avuto reazioni sistemiche.
Le
reazioni avverse sistemiche sono state
più comuni nella settimana dopo la seconda dose (40,9%), con
febbre nel 13,4%, rispetto al 7,9% dopo la prima dose.
Dalla versione online dello studio, riportiamo l'infografica sotto. Concludendo, i risultati preliminari sulla sicurezza sono simili a quelli degli studi clinici di pre-autorizzazione.

Efficacia del vaccino contro Covid-19 negli adolescenti
Il
vaccino BNT162b2 (Pfizer-BioNTech) ha dimostrato un'
elevata efficacia nella prevenzione dell'infezione da SARS-CoV-2 in studi randomizzati di Fase III controllati con placebo, in persone di età compresa tra 12 e 17 anni (indicati come adolescenti nel rapporto pubblicato in MMWR); tuttavia, i dati sull'efficacia del vaccino in termini reali
(VE) tra gli adolescenti sono limitati.
A partire dal dicembre 2021, il vaccino Pfizer-BioNTech è stato approvato dalla Food and Drug Administration (FDA) per gli adolescenti di età compresa tra 16 e 17 anni e con l'autorizzazione all'uso di emergenza della FDA per quelli di età compresa tra 12 e 15 anni.
Il
secondo studio condotto dal 25 luglio al 4 dicembre 2021, in una
potenziale coorte in Arizona, prende in esame
243 adolescenti di età compresa tra 12 e 17 anni. I ragazzi sono stati
testati ogni settimana per SARS-CoV-2 mediante RT-PCR, indipendentemente dai sintomi e all'insorgenza di COVID-19. La variante SARS-CoV-2 B.1.617.2 (Delta) era il ceppo predominante durante questo periodo di studio.
Durante lo studio:
- 190 adolescenti erano completamente vaccinati (≥14 giorni dopo aver ricevuto 2 dosi di vaccino Pfizer-BioNTech)
- 30 erano parzialmente vaccinati (con una 1 dose o con 2 dosi ma con la seconda dose completata <14 giorni prima)
- 66 non erano vaccinati.
Di tutti i partecipanti, il
51,4% erano ragazzi, il
74,5% aveva dai 12 ai 15 anni, l'
87,7% era bianco, il
74,5% non era ispanico e l'85,2% aveva un'assicurazione sanitaria privata.
Ventuno dei 243 partecipanti (8,6%) sono risultati
positivi al COVID-19, di cui 18 (85,7%) hanno riportato sintomi.
Utilizzando il modello a rischi proporzionali di Cox, il
VE stimato della vaccinazione completa Pfizer-BioNTech
per prevenire l'infezione da SARS-CoV-2 era
92% (95% CI = 79%-97%), aggiustato per caratteristiche sociodemografiche, informazioni sanitarie, frequenza di contatto sociale, uso della maschera, posizione e circolazione locale del virus.
La tabella 2 dello studio riporta il numero dei partecipanti, i giorni-persona totali, il numero di infezioni da SARS-CoV-2 confermate da RT-PCR per stato vaccinale, la stima dell’efficacia del vaccino Pfizer-BioNTech COVID-19 con la vaccinazione completa, per la prevenzione dell'infezione tra gli adolescenti idonei al vaccino di età 12-17 anni.
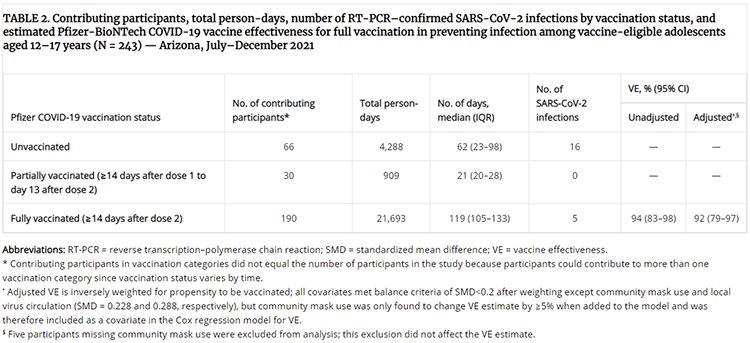
Questi risultati “real world” indicano che
2 dosi di vaccino Pfizer-BioNTech sono altamente efficaci nel
prevenire l'infezione da SARS-CoV-2 tra gli adolescenti dell'Arizona.
Per saperne di più:
 |
COVID-19 Vaccine Safety in Children Aged 5-11 Years - United States, November 3-December 19, 2021
Hause AM, Baggs J, Marquez P, Myers TR, Gee J, Su JR, Zhang B, Thompson D, Shimabukuro TT, Shay DK. MMWR Morb Mortal Wkly Rep. 2021 Dec 31;70(5152):1755-1760. doi: 10.15585/mmwr.mm705152a1. PMID: 34968370
|
 |
Interim Estimate of Vaccine Effectiveness of BNT162b2 (Pfizer-BioNTech) Vaccine in Preventing SARS-CoV-2 Infection Among Adolescents Aged 12-17 Years - Arizona, July-December 2021
Lutrick K, Rivers P, Yoo YM, Grant L, Hollister J, Jovel K, Khan S, Lowe A, Baccam Z, Hanson H, Olsho LEW, Fowlkes A, Caban-Martinez AJ, Porter C, Yoon S, Meece J, Gaglani M, Burns J, Mayo Lamberte J, Nakayima Miiro F, Bissonnette A, LeClair L, Kutty PK, Romine JK, Stefanski E, Edwards LJ, Ellingson K, Gerald JK, Bedrick EJ, Madhivanan P, Krupp K, Gerald LB, Thompson M, Burgess JL. MMWR Morb Mortal Wkly Rep. 2021 Dec 31;70(5152):1761-1765. doi: 10.15585/mmwr.mm705152a2. PMID: 34968373. |
Per approfondire:



